Résumé des expériences
Expérience sur la composition des larmes :
Objectif: Déterminer la composition des larmes
Expérience n°1 : Test de vérification de la présence d'eau
Objectif : Montrer la présence d'eau dans les larmes
Matériel : - une coupelle
- sulfate de cuivre anhydre
- larmes
Protocole :
1) Déposer un peu de sulfate de cuivre anhydre sur une coupelle.
2) Y verser quelques gouttes de larmes.
3) Patienter quelques instants.
4) Observer.

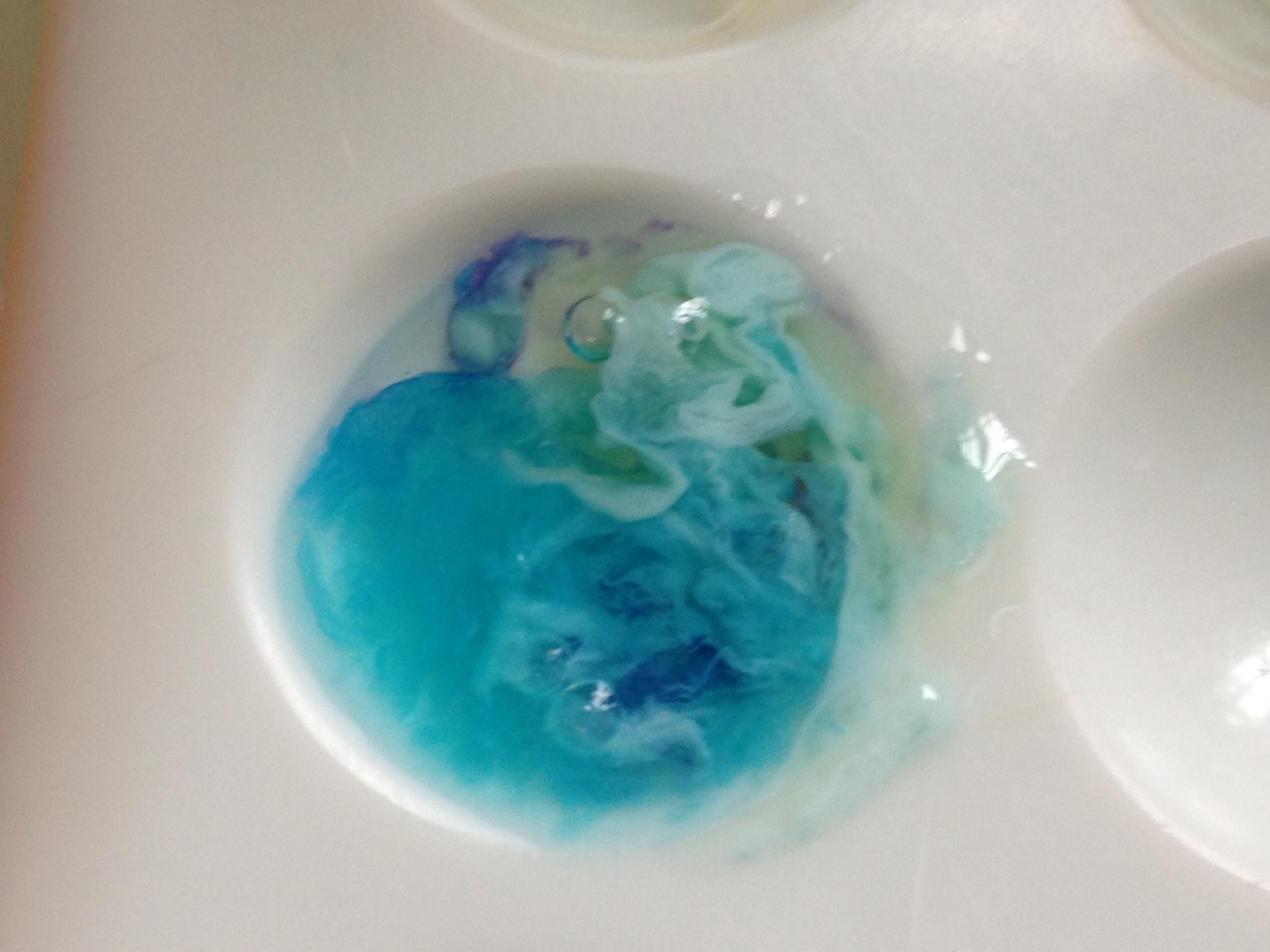
Observation : Le sulfate de cuivre anhydre est devenu bleu au contact des larmes.
Conclusion : Le sulfate de cuivre anhydre a pour propriété de se teindre en bleu lorsqu'il est en présence d'une solution composée d'eau. Donc les lames contiennent de l'eau de formule H2O.
Expérience n°2 : Test de vérification de la présence de chlorure
Objectif : Montrer la présence de chlorures dans les larmes
Matériel : - un tube à essai
- nitrate d'argent
- larmes
Protocole :
1) Déposer un peu de nitrate d'argent dans un tube à essai.
2) Y verser quelques gouttes de larmes.
3) Patienter quelques instants.
4) Observer.

Observation : Un précipité blanc qui noircit à la lumière est apparu.
Conclusion : Le nitrate d'argent a pour propriété de former un précipité blanc qui noircit à la lumière lorsqu'il est en contact avec une solution composée de chlorure. Donc les larmes sont contiennent des chlorures.
Expérience n°3 : Test de vérification de la présence de protéines
Objectif : Montrer la présence de protéines dans les larmes
Matériel : - un tube à essai
- hydroxyde de sodium (Na+ , OH-)
- sulfate de cuivre
- larmes
Protocole :
1) Verser quelques gouttes de larmes dans un tube à essai.
2) Ajouter de l'hydroxyde de sodium puis du sulfate de cuivre.
3) Patienter quelques instants.
4) Observer.
Observation : Une coloration violette apparaît.
Conclusion : Le rôle de la solution de Biuret est de se colorer en violet lorsqu'elle est en présence d'une solution composée de protéines. Donc les larmes sont composées de protéines.
Expérience n°4 : Test pH des larmes
Objectif : Déterminer le pH des larmes
Matériel : - bandelette pH
- larmes
Protocole :
1) Prendre une bande de papier pH.
2) Mettre dessus quelques gouttes de larmes.
3) Patienter quelques instants puis observer.
Observation : Le milieu de la bandelette pH est devenu vert.
Conclusion : Donc le pH d'une larme est d'environ 7.
Expérience 5 : Test de vérification de la présence de glucose
Objectif : Montrer la présence de glucose
Matériel : - larmes
- papier glucose
Protocole :
1) Prendre une bandelette glucose.
2) Mettre dessus quelques gouttes de larmes.
3) Patienter quelques instants puis observer (lire le résultat en s'aidant de l'échelle de couleur présente sur la boîte).
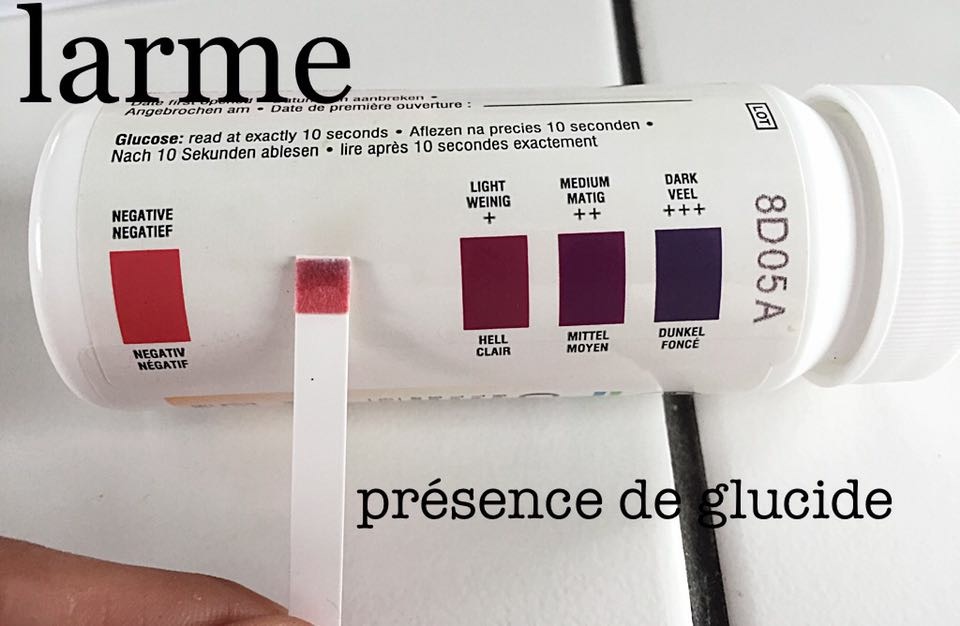
Observation : La bandelette de glucose a changé de couleur, elle est devenu violette.
Conclusion : Les larmes sont donc composées de glucose.
Expérience sur la composition des larmes artificelles et du sérum physiologique :
Objectif : Déterminer la composition des larmes artificielles et du sérum physiologique
Expérience n°1 : Test de vérification de la présence d'eau
Objectif : Montrer la présence d'eau dans les larmes artificielles et le sérum physiologique
Matériel : - deux coupelles
- sulfate de cuivre anhydre
- larmes artificielles
- sérum physiologique
Protocole :
1) Déposer un peu de sulfate de cuivre anhydre sur deux coupelles.
2) Verser sur la première quelques gouttes de larmes artificielles et sur la deuxième, quelques gouttes de sérum physiologique.
3) Patienter quelques instants.
4) Observer
Sérum physiologique: 
Larmes artificielles: 
Observation : Le sulfate de cuivre anhydre est devenu bleu au contact des larmes artificielles ainsi qu'au contact du sérum physiologique.
Conclusion : Les larmes artificielles et le sérum physiologique sont donc composés d'eau de formule H2O.
Expérience n°2 : Test de vérification de la présence de chlorure
Objectif : Montrer la présence de chlorures dans les larmes artificielles et du sérum physiologique
Matériel : - deux tubes à essai
- nitrate d'argent
- larmes artificielles
- sérum physiologique
Protocole :
1) Déposer un peu de nitrate d'argent dans deux tubes à essai.
2) Verser sur la première quelques gouttes de larmes artificielles et sur la deuxième quelques gouttes de sérum physiologique.
3) Patienter quelques instants.
4) Observer.
Larmes artificielles: 
Même réaction avec le sérum physiologique.
Observation : Un précipité blanc qui noircit à la lumière s'est formé au contact des larmes artificielles ainsi qu'au contact du sérum physiologique.
Conclusion : Les larmes artificielles et le sérum physiologique sont donc composés de chlorures.
Expérience n°3 : Test de vérification de l'abscence de protéines
Objectif : Montrer l'abscence de protéines dans les larmes artificielles et du sérum physiologique
Matériel : - deux soucoupes
- hydroxyde de sodium (Na+ , OH-)
- sulfate de cuivre
- larmes artificielles
- sérum physiologique
Protocole :
1) Verser quelques gouttes de larmes artificielles dans une soucoupe et du sérum physiologique dans une autre.
2) Ajouter de l'hydroxyde de sodium puis du sulfate de cuivre dans les deux soucupes.
3) Patienter quelques instants.
4) Observer.
Observation : Il n'y a aucun changement de couleurs
Conclusion : Les larmes artificielles et le sérum physiologique ne sont donc pas composés de protéines.
Expérience n°4 : Test pH des larmes
Objectif : Déterminer le pH des larmes artificielles et du sérum physiologique
Matériel : - bandelettes pH
- larmes artificielles
- sérum physiologique
Protocole :
1) Prendre deux bandes de papier pH.
2) Mettre sur une quelques gouttes de larmes artificielles et sur l'autre quelques gouttes de sérum physiologique.
3) Patienter quelques instants puis observer.
Sérum physiologique: 
Observation : Les bandelettes pH sont devenues vertes.
Conclusion : Donc les larmes artificielles et le sérum physiologique ont un pH neutre d'environ 7.
Expérience 5 : Test de vérification de la présence de glucose
Objectif : Montrer l’absence de glucose
Matériel : - larmes artificielles
- papier glucose
- sérum physiologique
Protocole :
1) Prendre deux bandelettes glucose.
2) Mettre sur l'une quelques gouttes de larmes artificielles et sur l'autre quelques gouttes de sérum physiologique.
3) Patienter quelques instants puis observer (lire le résultat en s'aidant de l'échelle de couleur présente sur la boîte).
Larmes artificielles: 
Même réaction avec le sérum physiologique.
Observation : Les bandelettes de glucose n'ont pas changé de couleur.
Conclusion : Les larmes artificielles et le sérum physiologique ne sont pas composés de glucose .
Expérience : La larme un antibiotique pour l’œil
Objectif : Déterminer un des rôle des larmes (antibiotique) à l'aide du lysozyme présent dans le blanc d’œuf.
Matériel : - blancs d’œufs
- micros-pipettes
- boites de pétries
- suspension bactérienne de B mégatérium et de E.Coli
- bec bunsen
- coupelles
- étaleur
- éthanol
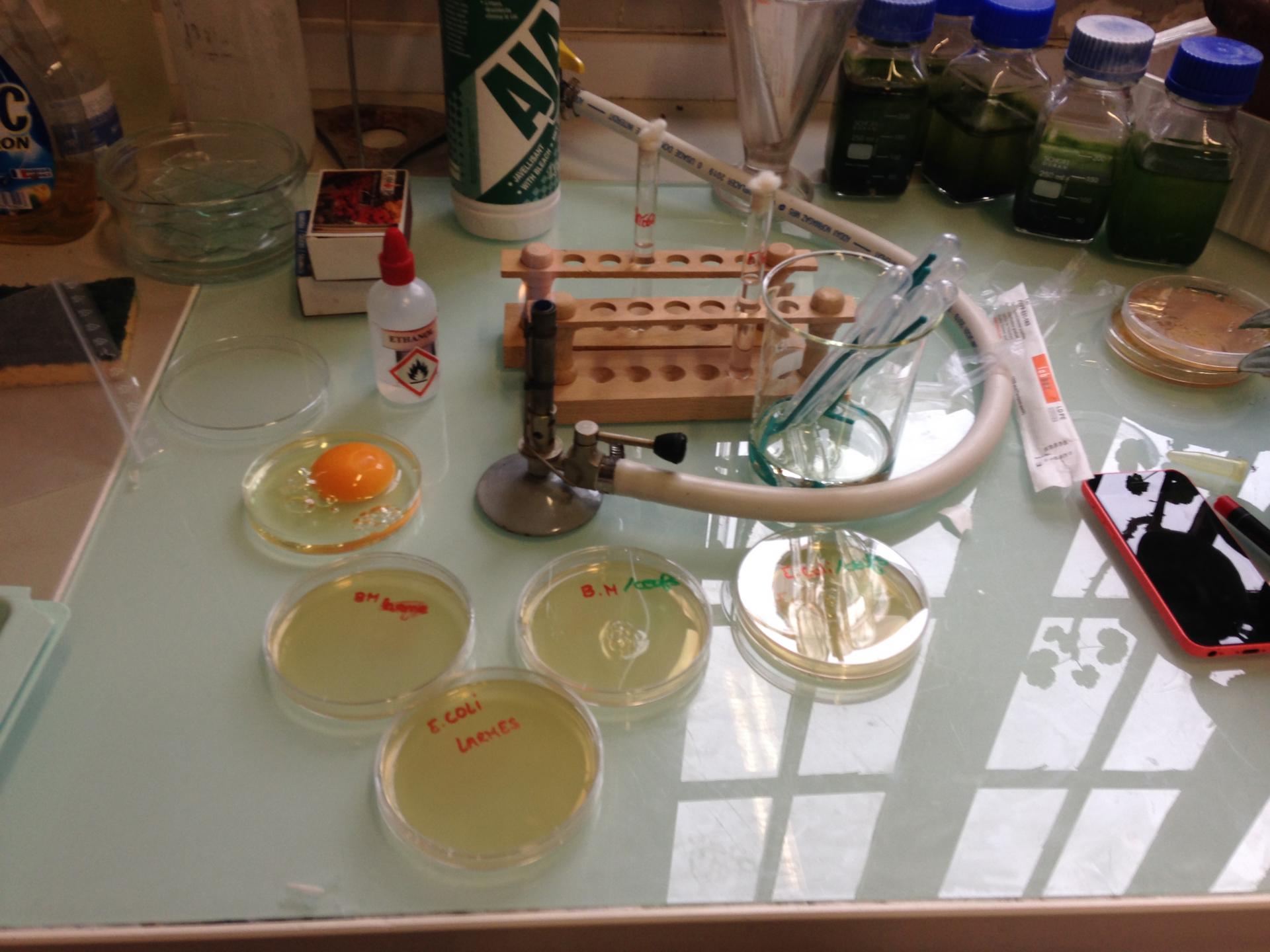
Protocole :
1) Se laver les mains avec de l'éthanol.
2) Dans un périmètre stérile d'environ 15 cm autour du bec bunsen casser l’œuf entier dans une coupelle afin de pouvoir prélever le blanc d’œuf (qui contient du lysozyme).
3) A l'aide d'une micro-pipette, absorber un peu de blanc d’œuf.
4) Ensuite déposer la boîte de Pétri à côté du bec bunsen à demi ouvert puis prendre la solution bactérienne d'E.Coli.
5) Après avoir bien agité la solution bactérienne, la verser sur la gélose de la boîte de Pétri.
6) A l'aide d'un étaleur stérile, répartir avec des mouvements circulaires la solution bactérienne pour qu'il y en ait sur toute la gélose.
7) Ensuite verser l'excédent de la solution E.Coli.
8) Ajouter à la solution bactérienne quelques gouttes de blanc d’œuf, récupéré précédemment, au milieu de la boîte, puis refermer la boîte de Pétri.
9) Puisque l'expérience consistait à comparer les résultats avec la solution d'E.Coli et la solution de B. Mégatérium, renouveler la même expérience mais avec une solution de B.Mégatérium.
L'expérience terminée nous la laissons reposer pendant 4-5 jours à température ambiante.
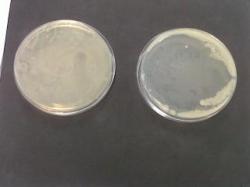
Observation : La boîte d'E. Coli est à gouche et celle de B.Mégaterium est à droite. On constate que pour la boite de pétrie contenant la suspension de B Mégatérium (Gram positive) , des champignons (bactéries) se sont formés autour du blanc d’œuf (présence de lysozyme). De plus, plus on s'éloigne du blanc d’œuf plus les champignons sont gros et inversement, plus on s'en rapproche plus les champignons sont petits voire inexistants.
Enfin, on observe que pour la boite de pétrie contenant la suspension d’E. Coli (Gram négative), contrairement à l'autre suspension, des champignons se sont formés sur la surface entière de la gélose même là où il y avait présence de blanc d’œuf (donc de lysozyme).
Conclusion : Donc le lysozyme est bien un antibiotique naturel, efficace sur les bactéries gram positive comme le B. Mégatérium mais non-efficace sur les bactéries gram négatif comme l'E.Coli.
Expérience : Hydrophobie et volume d'une larme
Objectif : Rendre une surface en verre hydrophobe pour faire tenir une goutte de larme en place afin de calculer son volume
Expérience n°1: Rendre une surface hydrophobe
Objectif: Rendre la plaque en verre hydrophobe
Matériel : - plaques en verre
- liquide vaisselle
- allumettes
- bougies chauffe plat
- larmes
- pipettes
Protocole :
1) Dégraisser la surface d'une plaque en verre au liquide vaisselle et l'essuyer.
2) Placer la flamme de la bougie chauffe-plat sous la plaque en verre de facon à y déposer de la suie (issue de la combustion) sur toute la surface.
3) A l'aide d'une pipette déposer une goutte de larmes sur la surface de la plaque où la fumée a laissé une trace noire.
Observation: La goutte est presque sphérique et ne s'écrase pas sur le verre.
Conclusion: Le verre est devenu hydrophobe à l'endroit où la fumée a léché celui-ci.
Expérience n°2: Calculer le volume
Objectif: Mesurer le diamètre d'une larme
Matériel: - pied à coulisse
- larme
- plaque de verre hydrophobe
Protocole:
1) Déposer la larme sur la surface hydrophobe.
2) Mettre le pied à coulisse horizontalement avec la goutte au milieu des deux barres.
3) Resserer le pied jusqu'à froler la larme.
4) Recupérer la mesure.
Conclusion: Le diamètre de la larme mesure 4,4 mm.
Rappel : La gélose est composée généralement d'un pH neutre ici d'un litre de Volvic, d'un acide aminé ici 7g de peptones, d'une source de vitamine ici 10g d'extrait de levure, d'une source de carbone ici 20g de glucose et enfin d'un gélifiant ici 15à20g d'agar agar. Tout cela est nécessaire pour favoriser l'apparition des bactéries.